Водород (Н) очень легкий химический элемент, с содержанием в Земной коре 0,9% по массе, а в воде 11,19%.
Характеристика водорода
По легкости он первый среди газов. При нормальных условиях безвкусен, бесцветен, и абсолютно без запаха. При попадании в термосферу улетает в космос из-за малого веса.
Во всей вселенной это самый многочисленный химический элемент (75% от всей массы веществ). Настолько, что многие звезды в космическом пространстве состоят полностью из него. Например, Солнце. Его основной компонент - водород. А тепло и свет это итог выделения энергии при слиянии ядер материала. Так же в космосе есть целые облака из его молекул различной величины, плотности и температуры.
Физические свойства

Высокая температура и давление значительно меняют его качества, но при обычных условиях он:
Обладает высокой теплопроводностью, если сравнивать с другими газами,
Нетоксичен и плохо растворим в воде,
С плотностью 0,0899 г/л при 0°С и 1 атм.,
Превращается в жидкость при температуре -252,8°С
Становится твердым при -259,1°С.,
Удельная теплота сгорания 120,9.106 Дж/кг.
Для превращения в жидкость или твердое состояние требуются высокое давление и очень низкие температуры. В сжиженном состоянии он текуч и легок.
Химические свойства
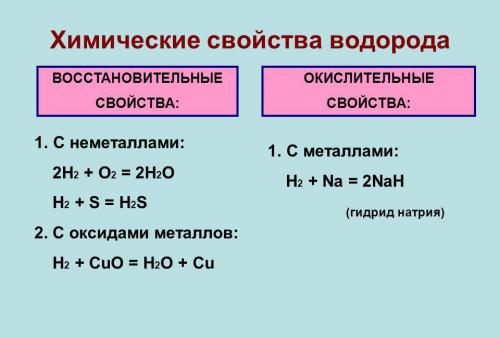
Под давлением и при охлаждении (-252,87 гр. С) водород обретает жидкое состояние, которое по весу легче любого аналога. В нем он занимает меньше места, чем в газообразном виде.
Он типичный неметалл. В лабораториях его получают путем взаимодействия металлов (например, цинка или железа) с разбавленными кислотами. При обычных условиях малоактивен и вступает в реакцию только с активными неметаллами. Водород может отделять кислород из оксидов, и восстанавливать металлы из соединений. Он и его смеси образуют водородную связь с некоторыми элементами.
Газ хорошо растворяется в этаноле и во многих металлах, особенно в палладии. Серебро его не растворяет. Водород может окисляться во время сжигания в кислороде или на воздухе, и при взаимодействии с галогенами.
Во время соединения с кислородом, образуется вода. Если температура при этом обычная, то реакция идет медленно, если выше 550°С - со взрывом (превращается в гремучий газ).
Нахождение водорода в природе
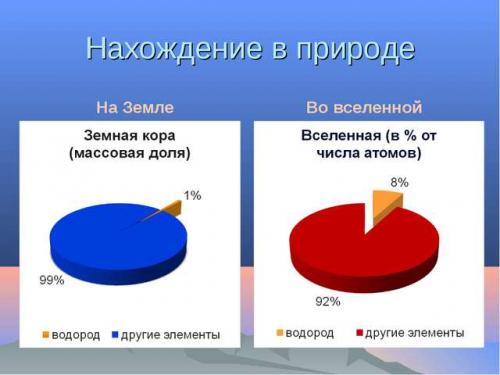
Хотя водорода очень много на нашей планете, но в чистом виде его найти нелегко. Немного можно обнаружить при извержении вулканов, во время добычи нефти и в месте разложения органических веществ.
Больше половины всего количества находится в составе с водой. Так же он входит в структуру нефти, различной глины, горючих газов, животных и растений (присутствие в каждой живой клетке 50% по числу атомов).
Круговорот водорода в природе
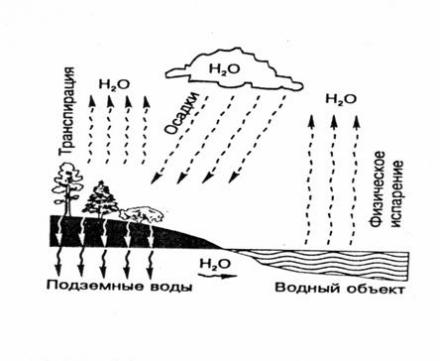
Каждый год в водоемах и почве разлагается колоссальное количество (миллиарды тонн) остатков растений и это разложение выплескивает в атмосферу огромную массу водорода. Так же он выделяется при любом брожении, вызываемом бактериями, сжигании и наравне с кислородом участвует в круговороте воды.
Области применения водорода
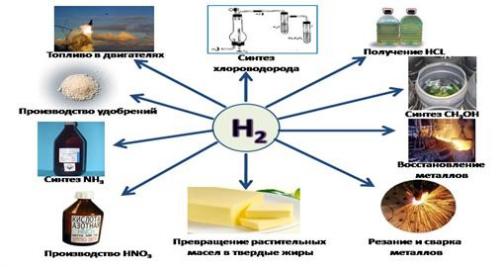
Элемент активно используется человечеством в своей деятельности, поэтому мы научились получать его в промышленных масштабах для:
Метеорологии, химпроизводства-
Производства маргарина-
Как горючее для ракет (жидкий водород)-
Электроэнергетики для охлаждения электрических генераторов-
Сварки и резки металлов.
Масса водорода используется при производстве синтетического бензина (для улучшения качества топлива низкого качества), аммиака, хлороводорода, спиртов, и других материалов. Атомная энергетика активно использует его изотопы.
Препарат «перекись водорода» широко применяют в металлургии, электронной промышленности, целлюлозно-бумажном производстве, при отбеливании льняных и хлопковых тканей, для изготовления красок для волос и косметики, полимеров и в медицине для обработки ран.
«Взрывной» характер этого газа может стать гибельным оружием - водородной бомбой. Ее взрыв сопровождается выбросом огромного количества радиоактивных веществ и губительно для всего живого.
Соприкосновение жидкого водорода и кожных покровов грозит сильным и болезненным обморожением.
Космические агентства и частные компании уже разрабатывают планы по отправке людей на Марс в ближайшие несколько лет, что в конечном итоге приведет к его колонизации. И с увеличением числа открытых землеподобных планет вокруг близлежащих звезд дальние космические путешествия становятся все более актуальными.
Однако людям нелегко выжить в космосе в течение длительного периода времени. Одной из основных проблем космического полета на большие расстояния является транспортировка достаточного количества кислорода для дыхания космонавтов и достаточного количества топлива для работы сложной электроники. К сожалению, в космосе практически нет кислорода, поэтому запасать его нужно на Земле.
Но новое исследование, опубликованное в Nature Communications , показывает, что можно производить водород (для топлива) и кислород (для дыхания) из воды, используя только полупроводниковый материал, солнечный (или звездный) свет и невесомость, что делает далекие путешествия более реальными.
Использование неограниченного ресурса Солнца для питания нашей повседневной жизни - одна из самых глобальных задач на Земле. Поскольку мы медленно отходим от нефти к возобновляемым источникам энергии, исследователи заинтересованы в возможности использования водорода в качестве топлива. Лучшим способом сделать это было бы разделение воды (H2O) на ее составляющие: водород и кислород. Это возможно с использованием процесса, известного как электролиз, который состоит в пропускании тока через воду, содержащую некоторое количество растворимого электролита (например, соли - прим. перев.). В результате вода распадается на атомы кислорода и водорода, которые выделяются каждый на своем электроде.

Электролиз воды.
Хотя этот метод технически возможен и известен уже не одно столетие, он все еще не стал легкодоступным на Земле, поскольку нам нужно больше инфраструктуры, связанной с водородом - например, заправочных станций водорода.
Водород и кислород, полученные таким образом из воды, могут также использоваться в качестве топлива на космическом корабле. Запуск ракеты с водой на самом деле был бы намного безопаснее, чем с дополнительным ракетным топливом и кислородом на борту, так как при аварии их смесь может быть взрывоопасной. Теперь же в космосе специальная технология сможет разделить воду на водород и кислород, которые, в свою очередь, могут быть использованы для поддержания дыхания и работоспособности электроники (например, с помощью топливных элементов).
Для этого есть два варианта. Один из них - это электролиз, как и на Земле, с использованием электролитов и солнечных батарей для получения тока. Но, увы, электролиз - очень энергозатратный процесс, а энергия в космосе и без того «на вес золота».
Альтернативой является использование фотокатализаторов, которые работают путем поглощения фотонов полупроводниковым материалом, размещенном в воде. Энергия фотона «выбивает» электрон из материала, оставляя в нем «дырку». Свободный электрон может взаимодействовать с протонами в воде с образованием атомов водорода. Между тем, «дырка» может поглощать электроны из воды с образованием протонов и атомов кислорода.
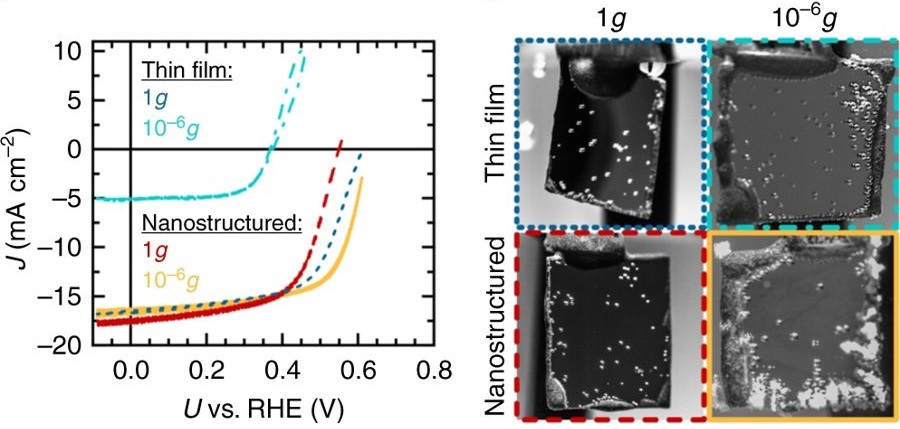
Процесс фотокатализа в земных условиях и при микрогравитации (в миллион раз меньше, чем на Земле). Как видно, во втором случае количество появляющихся пузырьков газа больше.
Этот процесс может быть повернут вспять. Водород и кислород могут быть рекомбинированы (объединены) с использованием топливного элемента, в результате чего «вернется» затраченная на фотокатализ солнечная энергия и образуется вода. Таким образом, эта технология - реальный ключ к дальним космическим путешествиям.
Процесс с использованием фотокатализаторов является наилучшим вариантом для космических путешествий, поскольку оборудование весит намного меньше, чем необходимое для электролиза. В теории, работать с ним в космосе также проще. Отчасти это объясняется тем, что интенсивность солнечного света вне атмосферы Земли существенно выше, так как в последней достаточно большая часть света поглощается или отражается по пути к поверхности.
В новом исследовании ученые сбросили полностью рабочую экспериментальную установку для фотокатализа с башни высотой в 120 метров, создав условия, называющиеся микрогравитацией. По мере того, как объекты падают на Землю в свободном падении, эффект гравитации уменьшается (но сама она никуда не исчезает, поэтому это и называют микрогравитацей, а не отсутствием гравитации - прим. перев.), поскольку нет сил, которые компенсируют притяжение Земли - таким образом, на время падения в установке создаются условия как на МКС.
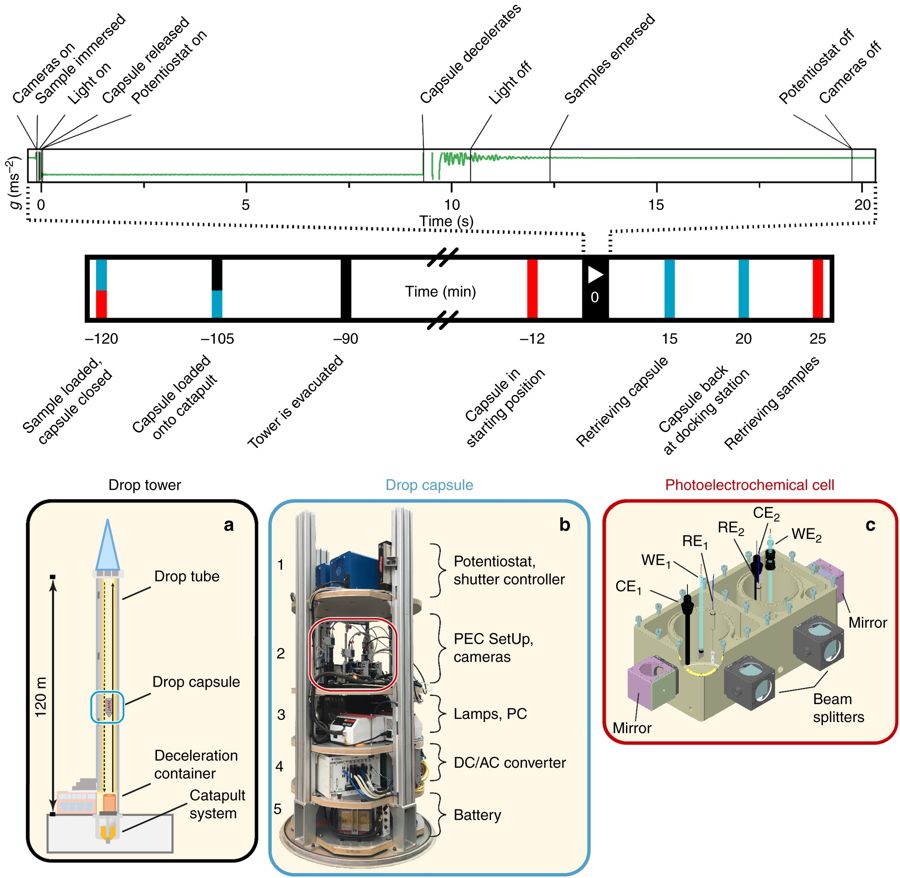
Экспериментальная установка и процесс эксперимента.
Исследователям удалось показать, что в таких условиях действительно возможно раcщепить воду. Однако, поскольку при этом процессе получается газ, то в воде образуются пузырьки. Важной задачей является избавление от пузырьков материала катализатора, поскольку они препятствуют процессу создания газа. На Земле гравитация заставляет пузырьки всплывать на поверхность (вода около поверхности плотнее пузырьков, что позволяет им плавать на поверхности), освобождая пространство у катализатора для образования следующих пузырьков.
При невесомости это невозможно, и пузырьки газа остаются на катализаторе или около него. Тем не менее, ученые скорректировали форму катализатора в наноразмерных масштабах, создав пирамидальные зоны, где пузырек может легко оторваться от вершины пирамиды и попасть в воду, не препятствуя процессу образования новых пузырей.
Но остается одна проблема. В отсутствие силы тяжести пузырьки останутся в жидкости, даже несмотря на то, что они вынуждены были покинуть катализатор. Гравитация позволяет газу легко выходить из жидкости, что имеет решающее значение для использования чистого водорода и кислорода. Без гравитации никакие пузырьки газа не плавают на поверхности и не отделяются от жидкости - вместо этого образуется аналог пены.
Это резко снижает эффективность процесса, блокируя катализаторы или электроды. Инженерные решения вокруг этой проблемы будут ключевыми для успешной реализации технологии в космосе - одно из возможных решений заключается в вращении установки: таким образом центробежные силы создадут искусственную гравитацию. Но, тем не менее, благодаря этому новому исследованию мы стали на шаг ближе к длительному космическому полету людей.
Астрофизики знают, что для звездообразования необходимо топливо. Современная теория гласит, что реки водорода — известные как «холодные потоки» — могут быть своего рода переправами водорода через межгалактическое пространство и, следовательно, подпитывать процесс звездообразования.
Спиральные галактики, как наш Млечный Путь, как правило, имеют довольно спокойный, но устойчивый темп звездообразования. Другие галактики, такие как NGC 6946, которая находится примерно в 22 млн. световых лет от Земли на границе созвездий Цефея и Лебедя, гораздо более активны в этом плане. Это поднимает вопрос о том, что является питательной средой для устойчивого формирования звезд в этой и аналогичных ей спиральных галактиках.
Предыдущие исследования ближайшего галактического пространства вокруг NGC 6946 с телескопа WSRT в Нидерландах выявили протянутое гало водорода. Однако, холодный поток мог быть сформирован водородом совсем из другого источника — газом из межгалактического пространства, который никогда не нагревался до высоких температур процессом рождения звезд.
Используя Green Bank Telescope (GBT), Пизано удалось обнаружить свечение, испускаемое нейтральным водородом, соединяющим NGC 6946 с его космическими соседями. Этот сигнал был просто ниже порога обнаружения других телескопов, но уникальные возможности GBT позволили ученому обнаружить это слабое излучение.
Астрономы уже давно предположили, что крупные галактики могут получать постоянный приток холодного водорода с помощью его откачки с других менее массивных компаньонов.
Дальнейшие исследования помогут подтвердить природу этого наблюдения и помогут пролить свет на возможную роль, которую холодные потоки играют в эволюции галактик.
Обобщающая схема «ВОДОРОД»
I.Водород – химический элемент
а) Положение в ПСХЭ
- порядковый номер №1
- период 1
- группаI(главная подгруппа «А»)
- относительная массаAr(Н)=1
- латинское название Hydrogenium (рождающийводу)
б) Распространённость водорода вприроде
| Водород - химический элемент. | В земной коре (литосфера и гидросфера) – 1% по массе(10 местосреди всех элементов) |
| АТМОСФЕРА - 0,0001% по числу атомов | |
| Самый распространённый элемент во вселенной – 92% от числа всех атомов(основная составная часть звёзд и межзвёздного газа) |
|
Водород – химический
элемент |
В соединениях | Н 2 О – вода (11% по массе) |
| СН 4 – газ метан (25% по массе) | ||
|
Органические вещества (нефть, горючие природные газы идругих)
В организмах животных и растений (то есть в составе белков,нуклеиновых кислот, жиров, углеводов и других) В теле человека в среднем содержится около 7 килограммов водорода. |
в) Валентность водорода в соединениях
II. Водород – простое вещество (Н 2)
Получение
|
1.Лаборатория(аппарат Киппа)
А) Взаимодействие металлов с кислотами: Zn + 2HCl= ZnCl2 + H2 соль Б) Взаимодействие активных металлов с водой: 2Na+ 2H2 O= 2NaOH+ H2 основание |
|
2.Промышленность
·Электролиз воды эл. ток 2H2 O=2H2 + O2 ·Из природного газа t, Ni CH 4 + 2H 2 O=4H 2 +CO 2 |
Нахождениеводорода в природе.
Водород широкораспространен в природе, его содержание в земной коре (литосфера и гидросфера) составляетпо массе 1%, а по числу атомов 16%. Водород входит в состав самогораспространенного вещества на Земле - воды (11,19% Водорода по массе), в составсоединений, слагающих угли, нефть, природные газы, глины, а также организмыживотных и растений (то есть в состав белков, нуклеиновых кислот, жиров,углеводов и других). В свободном состоянии Водород встречается крайне редко, внебольших количествах он содержится в вулканических и других природных газах.Ничтожные количества свободного Водорода (0,0001% по числу атомов) присутствуютв атмосфере. В околоземном пространстве Водород в виде потока протонов образуетвнутренний (протонный) радиационный пояс Земли. В космосе Водородявляется самым распространенным элементом. В виде плазмы он составляет околополовины массы Солнца и большинства звезд, основную часть газов межзвезднойсреды и газовых туманностей. Водород присутствует в атмосфере ряда планет и вкометах в виде свободного Н 2 , метана СН 4 , аммиака NH 3 ,воды Н 2 О, радикалов. В виде потокапротонов Водород входит в состав корпускулярного излучения Солнца и космическихлучей.
Существуют три изотопа водорода:
а) легкий водород – протий,
б) тяжелый водород – дейтерий (D),
в) сверхтяжелый водород – тритий (Т).
Тритий неустойчивый(радиоактивный) изотоп, поэтому в природе он практически не встречается.Дейтерий устойчив, но его очень мало: 0,015% (от массы всего земного водорода).
Валентностьводорода в соединениях
В соединениях водородпроявляет валентностьI.
Физическиесвойства водорода
Простое веществоводород (Н 2) – это газ, легче воздуха, без цвета, без запаха, безвкуса, t кип = – 253 0 С, водород в воде нерастворим , горюч. Собирать водород можно путем вытеснениявоздуха из пробирки или воды. При этом пробирку нужно перевернуть вверх дном.
Получениеводорода
В лаборатории водородполучают в результате реакции
Zn + H 2 SO 4= ZnSO 4 + H 2.
Вместо цинка можноиспользовать железо, алюминий и некоторые другие металлы, а вместо сернойкислоты – некоторые другие разбавленные кислоты. Образующийся водород собираютв пробирку методом вытеснения воды (см. рис. 10.2 б) или просто вперевернутую колбу (рис. 10.2 а).
В промышленности в большихколичествах водород получают из природного газа (в основном это метан) привзаимодействии его с парами воды при 800 °С в присутствии никелевогокатализатора:
CH 4 + 2H 2 O = 4H 2 +CO 2(t, Ni)
или обрабатывают привысокой температуре парами воды уголь:
2H 2 O + С =2H 2 + CO 2 . (t)
Чистый водород получаютиз воды, разлагая ее электрическим током (подвергая электролизу):
2H 2 O = 2H 2 + O 2 (электролиз).
Бесцветный горючий газ без запаха. Плотность водорода при нормальных условиях равна 0,09 кг/м3- плотность по воздуху - 0,07 кг/м3- теплота сгорания-28670 ккал/кг- минимальная энергия зажигания - 0,017 мДж. С воздухом и кислородом образует взрывоопасную смесь. Смесь с хлором (1:1) на свету взрывается- с фтором водородсоединяется со взрывом в темноте- смесь с (2:1) - гремучий газ. Пределы взрываемости: с 4 - 75 об. %, с кислородом 4,1 - 96 об. %.
В день, когда его запасы иссякнут, жизнь во Вселенной прекратится. Вещество, без которого жизнь невозможна, «сидит» в самом центре нашей планеты - в ядре и вокруг него, и оттуда «мигрирует» наружу. Этот газ - начало всех начал. Его название - «водород».
Водород находится в ядре и вокруг него. Далее идет плотная мантия. Но этот газ спокойно мигрирует через толщу горных пород. Когда Земля была молода, водорода в глубинах имелось значительно больше, и из глубин он уходил наружу по всей Земле. Когда же его стало меньше, процесс относительно стабилизировался, и водород стал «выходить» по особым зонам, вдоль разломов океанических хребтов.
Конечно, современная жизнь на Земле возникла при определенном потенциале кислорода. Но если быть объективным, то началом всех начал на нашей планете мы обязаны водороду. Именно динамический цикл водорода, процесс его поступления из недр Земли, а не углерода, как было принято считать раньше, и стал источником зарождения жизни на Земле.
Водород и Вселенная
Обычно для того, чтобы подчеркнуть значение того или иного элемента, говорят: если бы его не было, то случилось бы то-то и то-то. Но, как правило, это не более чем риторический прием. А вот водорода может когда-нибудь действительно не стать, потому что он непрерывно сгорает в недрах звезд, превращаясь в инертный .
Водород - самый распространенный элемент космоса. На его долю приходится около половины массы Солнца и большинства других звезд. Он содержится в газовых туманностях, в межзвездном газе, входит в состав звезд. В недрах звезд происходит превращение ядер атомов водорода в ядра атомов гелия. Этот процесс протекает с выделением энергии- для многих звезд, в том числе для Солнца, он служит главным источником энергии.
Каждую секунду Солнце излучает в космическое пространство энергию, эквивалентную четырем миллионам тонн массы. Эта энергия рождается в ходе слияния четырех ядер водорода, протонов, в ядро . При «сгорании» одного грамма протонов выделяется в двадцать миллионов раз больше энергии, чем при сгорании грамма каменного угля. На Земле такую реакцию еще никто не наблюдал: она идет при температуре и давлении, существующими лишь в недрах звезд и еще не освоенных человеком.
Мощность, эквивалентную ежесекундной убыли массы в четыре миллиона тонн, невозможно представить: даже при мощнейшем термоядерном взрыве в энергию превращается всего около килограмма вещества. Однако скорость процесса, т.е. количество ядер водорода, превращающихся в ядра гелия в одном кубическом метре за одну секунду, мала. Поэтому и количество энергии, выделяющейся за единицу времени в единице объема, невелико. Таким образом, получается, что удельная мощность Солнца ничтожно мала – много меньше, чем мощность такого «тепловыделяющего устройства», как сам человек! И расчеты показывают, что Солнце будет светить, не ослабевая, еще по меньшей мере тридцать миллиардов лет. На наш век хватит.
Рождающий воду
Водород был открыт в первой половине XVI века немецким врачом и естествоиспытателем Парацельсом. В трудах химиков XVI–XVIII вв. упоминался «горючий газ» или «воспламеняемый воздух», который в сочетании с обычным давал взрывчатые смеси. Получали его, действуя на некоторые металлы (железо, цинк, олово) разбавленными растворами кислот - серной и соляной.
Первым ученым, описавшим свойства этого газа, был английский ученый Генри Кавендиш. Он определил его плотность и изучил горение на воздухе, однако приверженность теории флогистона* помешала исследователю разобраться в сути происходящих процессов.
В 1779 г. Антуан Лавуазье получил водород при разложении воды, пропуская ее пары через раскаленную докрасна железную трубку. Лавуазье также доказал, что при взаимодействии «горючего воздуха» с кислородом образуется вода, причем газы реагируют в объемном соотношении 2:1. Это позволило ученому определить состав воды - Н2О. Название элемента – Hydrogenium – Лавуазье и его коллеги образовали от греческих слов «гидор» - вода и «геннао» – рождаю. Русское наименование «водород»предложил химик М. Ф. Соловьев в 1824 году - по аналогии с ломоносовским «кислородом».
Водород - бесцветный газ без вкуса и запаха, слабо растворимый в воде. Он в 14,5 раз легче воздуха - самый легкий из газов. Поэтому водородом раньше наполняли аэростаты и дирижабли. При температуре -253°С водород сжижается. Эта бесцветная жидкость - самая легкая из всех известных: 1 мл ее весит меньше десятой доли грамма. При -259°С жидкий водород замерзает, превращаясь в бесцветные кристаллы.
Молекулы Н2 настолько малы, что способны легко проходить не только через мелкие поры, но и сквозь металлы. Некоторые из них, например, никель, могут поглощать большое количество водорода и удерживать его в атомарном виде в пустотах кристаллической решетки. Нагретая до 250°С палладиевая фольга свободно пропускает водород- этим пользуются для тщательной очистки его от других газов.
С растворимостью водорода в металлах связана его способность диффундировать через металлы. Кроме того, будучи самым легким газом, водородобладает наибольшей скоростью диффузии: его молекулы быстрее молекул всех других газов распространяются в среде другого вещества и проходят через разного рода перегородки.
Водород - активное вещество, легко вступающее в химические реакции. При его горении выделяется много теплоты, а единственным продуктом реакции является вода: 2Н2 + О2 = 2Н2О. О столь экологически чистом топливе можно только мечтать!
Сегодня (правда, пока что ограниченными партиями) уже выпускаются автомобили с водородными двигателями. Это BMW Hydrogen 7, в котором в качестве топлива используется жидкий водород- автобус Mercedes Citaro и легковой автомобиль Mazda RX-8 Hydrogen, работающий одновременно на бензине и водороде. А компания Boeing разрабатывает беспилотный самолёт большой высоты и продолжительности полёта (High Altitude Long Endurance (HALE). На самолёте установлен водородный двигатель производства Ford Motor Company. Однако развитие водородной энергетики сдерживает высокая степень риска при работе с этим газом, а также трудности его хранения.
Опыт, едва не стоивший жизни
С кислородом воздуха водородобразует взрывчатую смесь –- гремучий газ. Поэтому при работе с водородом необходимо соблюдать особую осторожность. Чистый водород сгорает почти бесшумно, а в смеси с воздухом издает характерный громкий хлопок. Взрыв гремучего газа в пробирке не представляет опасности для экспериментатора, однако при использовании плоскодонной колбы или посуды из толстого стекла можно серьезно пострадать.
Водород имеет двойственную химическую природу, проявляя как окислительную, так и восстановительную способность. В большинстве реакций он выступает в качестве восстановителя, образуя соединения, в которых его степень окисления равна +1. Но в реакциях с активными металлами он выступает в качестве окислителя: его степень окисления в соединениях с металлами равна -1.
Таким образом, отдавая один электрон, водород проявляет сходство с металлами первой группы периодической системы, а присоединяя электрон, – с неметаллами седьмой группы. Поэтому водород в периодической системе обычно помещают либо в первой группе и в то же время в скобках в седьмой, либо в седьмой группе и в скобках в первой.
Использование и получение водорода
Используется водород в производстве , метанола, хлороводорода, для гидрирования растительных жиров (при выработке маргарина), также для восстановления металлов (молибдена, вольфрама, индия) из оксидов. Водород-кислородным пламенем (3000°С) сваривают и режут тугоплавкие металлы и сплавы. Жидкий водород служит ракетным топливом.
При гидрогенизации угля и нефти бедные водородом низкосортные виды топлива превращаются в высококачественные.
Водород используют для охлаждения мощных генераторов электрического тока, а его изотопы находят применение в атомной энергетике.
В промышленности водород получают электролизом водных растворов солей (например, NaCl, Na2CO4), а также при конверсии твердого и газообразного топлива – угля и природного газа. Процессы конверсии протекают при температуре порядка 1000°С в присутствии катализаторов. Получаемая при этом газовая смесь называется синтез-газом.
Почти в каждой домашней аптечке имеется пузырек 3-процентного раствора перекиси водородаН2О2. Его используют для дезинфекции ран, остановке кровотечений.
В зависимости от назначения технический водород выпускается в сжатом и несжатом виде двух марок:
Водород газообразный марка «А»- используется в электронной, фармацевтической, химической промышленностях, в порошковой металлургии: для осаждения тугоплавких соединений из окислов металлов- при спекании изделий из порошковых материалов, содержащих хром и нержавеющие стали.
- используется в энергетике, электронной, химической, цветной металлургии, фармацевтической промышленности.








Добавить комментарий